第3章―7 代謝系
浸透圧制御
生物の生存にとって体液の塩類等の濃度を一定に保つことは重要である。しかし、水圏に棲息する動物は恒常性を保つ上で浸透圧というやっかいな問題に直面する。海水の環境では、脊椎動物の多くはその体液の濃度が環境水より低いため体内と体外の浸透圧差により鰓や体表を通して体内の水が流出し、塩類が流入する。一方低浸透圧の淡水の環境では、環境水より体液の濃度が高いので鰓や体表を通して体内に水が流入し、塩類が流出する。そのため周囲環境からの水やイオンの流出入を制御し、体を構成する各細胞が活動できるように体液の恒常性を保つ必要がある(Evans 2008)。
一方、水圏から陸圏に棲息場所を移す場合、浸透圧の問題はなくなるが、体表からの水の散逸を抑制する必要がある。そのために適量の水や塩類等を食餌により摂取し、腎臓を経由して排出される塩類や水の量を調整することで、恒常性を維持している。
水圏に棲息する動物は体内外の浸透圧差に対して4つの方法で適応している。体液の濃度を環境水のイオン濃度とほぼ同じに保ち体内外の浸透圧差を小さくする浸透圧順応型と体液濃度を体を構成する各細胞の活動に適したほぼ海水の1/3程度の一定値に保つ浸透圧調整型に大別される。前者はさらに海生の多くの無脊椎動物や原始的な脊椎動物が採用している方式と軟骨魚類が採用している方式の2つに分けられる。後者の浸透圧調整型は海水適応と淡水適応の2つに分けられる。以下に4つの方式の各々に関して述べる。
一つ目は、現生の無顎類ヌタウナギに見られる浸透圧順応型である。体液中のNaイオンやClイオンといった一価イオンの濃度を海水のそれとほぼ同じにし(Robertson 1974)、体内からの脱水を防ぐとともに、細胞内にグリシンやアラニンといった中性のアミノ酸を蓄積して細胞内からの脱水を抑制し、海水中での生存を可能にしている(Currie & Edwards 2010)。即ち、体を構成する個々の細胞レベルで浸透圧に対応していることになる。
細胞レベルでホメオスタシスを保つ方式は、多細胞生物になる以前の永い単細胞時代に獲得したものであり、海を棲息場所としていた古生代のヌタウナギは細胞レベルでホメオスタシスを保つ方式を引き継いでいたと考えられる。現生ヌタウナギも同様海での棲息に順応型で適応している。現生種と同様古生代のヌタウナギも浸透圧調整ホルモン遺伝子は持っていたとされるが、それを活用した新たな現生の無顎類ヌタウナギシステムを進化させる必要が無かったのであろう。あるいは逆に新たなシステムを開発しなかったために現在の生態系で主要な位置を占められなかったともいえよう。
二つ目の浸透圧順応型は、大部分の現生軟骨魚類とシーラカンスが採用している方法であり、体液や細胞内に尿素を蓄積し、体液を海水よりわずかに高張に保ち、これにより体内と海水との浸透圧差を小さくしている。アンモニアよりも毒性が低いとはいえ多量の尿素を体内に保持することは生体にとって好ましくないが、トリメチルアミンオキサイドなどのメチルアミン類を同時に持つことで尿素を無害化し、細胞内の酵素活性を正常に維持している。
硬骨魚類は後述するように浸透圧調整機能を持つ塩類細胞と腎臓を持っているが、軟骨魚類も直腸に塩類細胞に似た機能を持つ直腸腺と鰓に塩類細胞を持っており、これらと腎臓によって一価イオン、二価イオンを排出し、浸透圧の微調整を行っていると思われる。
三つ目は、現生海生魚類の大部分を占める硬骨魚類が採用している浸透圧調整法である。これら魚類の体内浸透圧は海水の1/3前後であるため、海水中では常に塩類の体内への流入と体内水分の流出にさらされている。ホメオスタシスを保つために海水を多量に飲んで水を補給しているが、同時に種々のイオンが体内に大量に入り、神経や情報伝達系が機能しなくなる恐れがある。そのため過剰に採取された塩類イオンのうちナトリウムイオンなどの一価イオンを主に鰓にある塩類細胞から排出し、二価イオンを腎臓から少量の尿と一緒に排出して体液の浸透圧が海水の1/3になるように調整している(Kaneko 2006)(Hyodo et al. 2004)。
四つ目は浸透圧調整型の淡水適応である。淡水性の硬骨魚類も海生の魚類と同じ程度の体液濃度であり、そのため塩類の体内からの流出と体内への水の流入にさらされる。流入してくる水を腎臓で尿にして排出することで、体液濃度を海水のおよそ1/3になるように調整している。また、淡水は塩類イオン濃度が海水に比べると非常に低いので、淡水性の魚類にとっては塩類イオンの体内への採取が問題になるが、食餌からの採取のほかに海生魚類の塩類細胞とは逆の機能を持つ、即ち淡水から塩類イオンを体内に取り込む塩類細胞を進化させて対応しているとされる。
塩類細胞
海生の魚類では浸透圧調整のために大量の海水を飲む必要があるが、それに伴い体内には過剰な塩類イオンが入りこむ。この過剰塩類を体外に除去する必要がある。一方塩類イオンが少ない淡水域に棲息する魚類では不足する塩類を環境水から体内に取り込む必要がある。こういった塩類イオンを能動的に移動する機能を持つ細胞が塩類細胞であり、塩類を移動させるためのエネルギーを供給するミトコンドリアを多量に含んでいる。塩類細胞をmitochondria rich cellとも呼ぶ。塩類細胞は主に鰓弁部上皮に存在する。鰓弁部は効率化のために複雑な管系構造を持ち、表面積を増やしている。
最近広塩性のモザンビーク・テラピア等における淡水適応時、および海水適応時の塩類細胞の機能が調べられ、塩類細胞におけるイオン移送のメカニズムが明らかになってきた。海水型、淡水型などいくつかのモデルが提案されている(Hwang & Lee 2007)(Tresguerres et al. 2006)(Parks et al. 2009)(Bartels & Potter 2004)(Sakamoto et al. 2001)(McCormick 2001)(Hiroi et al. 2005)。
図1に淡水型と海水型の相関とイオン移動に関する塩類細胞モデルを示す。Ⅰ~Ⅲが淡水型であり、Ⅳが海水型である。テラピアを淡水から海水に移すと約12時間でTypeⅣが現れ、24時間~48時間かけて数が増え、一方TypeⅢは消失する。淡水から海水に移すと約12時間でTypeⅣが減少しほぼ48時間で消失するとともにTypeⅢが増加し、TypeⅡが出現し数を増やす。TypeⅠは淡水でも海水でも存続する。従って、TypeⅠは未分化型であり、TypeⅡはイオン吸収性の淡水型、TypeⅢはTypeⅣの休眠型でTypeⅡとは異なる機構のイオン吸収性を持つ。TypeⅣはイオン分泌性の海水型である。
海水型では、細胞底部にあるNa+、K+-ATPaseにより細胞内外にNa+濃度勾配が形成される。この勾配によって細胞内にNa+、K+、Cl―が移送され、さらにCl―が細胞頂部からcystic fibrosis transmembrane conductance regulator (CFTR)を通って体外に排出される(広瀬茂久、中田勉 2006)。淡水型では細胞底部にClイオンチャンネルの存在が必要であり、このイオンチャンネルの活性にはCortisol等のホルモンが関与しているとされるが、その詳細はまだ不明のようである(Sakamoto et al. 2001)(Takei 2008)。

TypeⅠ~Ⅲが淡水型であり、TypeⅣが海水型。赤:Na+/K+-ATPase、シアン:Na+/K+/2Cl―共輸送部(NKCC)、緑:cystic fibrosis transmembrane conductance regulator (CFTR)。簡単のためNa+、Cl―イオンの動きに注目し、K+のchannel recycling は記載していない。灰色:Cl―チャンネル。4種の塩類細胞間の推測される相関を矢印A~Eで示す。AC:アクセサリー細胞 From Hiroi et al. 2005
塩類細胞は海生魚類では体内の過剰な塩類を排出する機能を持ち、淡水性の魚類では必要な塩類を塩類細胞によって摂りいれるとされる(Hiroi et al. 2005)。しかし、淡水性条鰭類の塩類細胞によるミネラルイオン調整(吸収)に関しては議論が継続中である(Hwang & Lee 2007)(Evans 2008)。例えばCaイオンを従来考えられていたほどには塩類細胞によって吸収されないようである( Shahsavarani et al. 2006)。しかし、一般にCaイオンは淡水でも多量に含まれており、また摂食により腸からの吸収も可能である。骨組織をCaイオンのリザーバーにする必要性は陸棲脊椎動物ほど大きくなく、棘魚類のように骨によるCaイオン保留機能が無い軟骨主体の魚類でも淡水に侵出できたのであろう。
腎臓
腎臓の機能は、本来は水と塩分の調整である(Ogasawara & Ichikawa 2009)。羊膜類の発生において見られる腎臓の形成過程は、腎臓の進化の過程を反映していると思われる。発生時における腎臓は前腎、中腎、後腎の順に形成され、後の腎が形成されると前に形成された腎は退化する。これら3種の腎は中胚葉の腎節に由来し、体の背側の体軸に沿って左右に対となって伸長する部分から分化して形成される。
この2対の最前方から最初に前腎が分化する。前腎では腎細管の先端がラッパ状に広がって並んで形成され、そのラッパ状開口の先に腎糸球体様:glomusの小器官が形成され、体腔を介して腎管につながる。無脊椎動物ヌタウナギの腎臓はこの段階に対応している。前腎の後方に中腎が形成されると前腎は退化する。中腎ではラッパ状開口もあるが腎糸球体とこれをラッパ状開口部が取り囲んだボーマン嚢からなるマルピギー小体の形成が見られる。各ラッパ状開口と各マルピギー小体の小管は次第に集まって中腎小管につながる。中腎は魚類や両生類の成体に見られる腎臓の構造である。中腎の後方に後腎が形成されると中腎は退化する。後腎では多数のマルピギー小体が形成され、各マルピギー小体からの腎細管は集まって集合管となる。羊膜類の腎臓は後腎から成長する。

左;前腎の形成 中;中腎の形成と前腎の消失 右;後腎の形成と中腎の消失
マルピギー小体から集合管につながる腎尿細管は、近位尿細管、ヘンレレープ、遠位尿細管の3部分からなり、各々ボーマン嚢で濾し取られた源尿から必要要素を再度吸収する機能を持つ。腎尿細管は生息環境によって形態が異なり、例えば海生魚類では1価イオンの再吸収を行う遠位尿細管が欠如している場合もある。また、軟骨魚類の腎尿細管は尿素の有効活用のために非常に長くて複雑な構造をしている(兵頭 2003)。

左端がボーマン嚢、右端が集合管につながる
左端がボーマン嚢、右端が集合管につながる
古生代の魚類における恒常性維持
軟骨魚類やシーラカンス等一部を除くと、現生魚類の多くは体内イオン濃度をほぼ海水のイオン濃度の1/3程度に保つために鰓や塩類細胞、あるいは腎臓により浸透圧調整を行っている。これらの器官はNPs:natriuretic peptidesなどの浸透圧調整ホルモンによって制御されている。
現生ヤツメウナギは淡水性の硬骨魚と類似した浸透圧調節機構をもっている。古生代に無顎類ヌタウナギより遅れて545Myaには出現したと考えられるヤツメウナギは当時は海生であり(Shu et al. 1999)、その後淡水域に進出している。従って、初期のヌタウナギは浸透圧調整ホルモン遺伝子を持っていたと予想され、海生から淡水へと侵出したヤツメウナギが、現生淡水性魚類に類似した浸透圧調整ホルモンを産生していた可能性は大きいと考えられる(Bartels & Potter 2004)。
ヤツメウナギ以外にも古生代に海生であった棘魚類、それにあまり多くはないが板皮類はいずれも淡水域にも進出している。従って古生代の魚類は既に浸透圧調整機能を保持していた可能性がある。また、体液イオン濃度を海水のほぼ1/3に保っている現生四肢類や条鰭類の共通祖先である初期硬骨魚類も同じ体液イオン濃度であったと考えられる。即ち、古生代の硬骨魚類も海生にせよ淡水生にせよ浸透圧調整を行っていたと考えられ、浸透圧調整ホルモン類も機能していたと考えられる。
体液イオン濃度を海水のほぼ1/3に保つ魚類は浸透圧調整型であり、浸透圧が変化した場合浸透圧を調整する専用の器官により体液濃度が保たれるので、体を構成する各細胞は浸透圧変化の影響をほとんど受けないで済む。一方、軟骨魚類は浸透圧順応型であり、浸透圧が変化した場合、体液や細胞内の浸透圧を総て変える必要があり、従って浸透圧順応型の方が浸透圧調整型よりも浸透圧変化への対応がより困難と考えられる。淡水に適応している軟骨魚類が少ない一因は、体内浸透圧を淡水に合わせるのが困難なためと考えられる。
古生代の初期魚類の分岐時期や海・淡水の分布や放散を考慮すると、板皮類、棘魚類の浸透圧変化への対応を類推することが出来ると思われる。化石記録から、板皮類は主に海の湾岸を生息場所にして多様化していることが分かっている。一方、棘魚類は最初は海に出現したが、ほどなく淡水域に進出し、主に淡水域で放散・繁栄している。
板皮類と軟骨魚類はオルドビス紀末には出現しており、最近板皮類のarthrodireが胎生であったことが明らかにされ(Long et al. 2009)、板皮類と軟骨魚類の類縁性が再確認された。恐らく板皮類も当時の軟骨魚類と同様尿素により体液の浸透圧を高める浸透圧順応型の方式を採用していたと思われる。淡水域に進出するには、体を構成している総ての細胞の内部機能を変える必要があり、このため板皮類も軟骨魚類と同様に淡水域への進出はそれほど容易ではなかったと思われる。
一方、海生として出現した棘魚類は後に淡水域へ進出し繁栄しており、板皮類や軟骨魚類より淡水域への進出が容易だったと思われる。従って、棘魚類は初期硬骨魚類と同様体液イオン濃度を海水の約1/3に保つ浸透圧調整型の方式を採用していた可能性がある。
なお、汽水域のように急激に塩分濃度が変化する場所では板皮類は強固な外皮により、軟骨魚類は直腸腺などで微調整することにより、一時的な塩分濃度変化に対応したと考えられる。ほぼ海水と同濃度の体液を持っているヌタウナギでは体表の粘液で一時的な外界の塩分濃度変化に対応していたであろう。
初期魚類進化の場は海だったのか、淡水だったのか?
初期脊椎動物が海域で進化したのか、淡水域で進化したのかに関する議論が長いこと為されてきた(Bray 1985)(Griffith 1987)。多くの初期魚類化石が淡水域で積層したと考えられたOld Red Sandstoneから出土していた。また海で堆積した地層からも化石が出土するが、成体がほとんどであり、海生であったにしても現生の原始的魚類の生活史と同様に淡水で繁殖し幼体時期を過ごした後に海へ移動して成体になったと考えられた(Griffith 1987)。
Smithは「腎臓に見られる糸球体は過剰な水の存在、即ち淡水棲息を裏付ける。軟骨魚類は四肢類以上に複雑な腎臓であるが、糸球体を持つ腎臓なのでかっては淡水性であったし、軟骨魚類の祖先とされる板皮類も最初は淡水性であった」と主張している。この考えに基づきローマーは、「現生海生魚類では、体液の塩類濃度が高くなるためポンプによる水の排出は必要ないはずなのに働いている。この不都合を解消するために二つの方法を開発した。一つは硬骨魚類に見られる塩類細胞であり、二つ目はサメ類に見られるように尿素濃度を高めて体外の塩類濃度と釣り合いを保つ方法である。こういった特殊な機能を発達させたことを説明できるのは、このような腎臓を発達させた祖先的脊椎動物は淡水中に棲んでいたからである」と考えた。そして「ポンプで絶えず水をくみ出す脊椎動物の腎臓は、淡水に棲む魚において発達したものである」と結論した。
ローマーの仮説に基づくと、「古生代の初期魚類は淡水に棲息しており、塩類細胞を持っていなかった。そのため海に進出するときに、塩類細胞を獲得するか、軟骨魚類のように尿素によって浸透圧に対応する必要があった」、と結論される。従って、軟骨魚類を含め初期魚類は淡水域に棲息しており、ポンプ機能の腎臓を持っており、従ってその体液イオン濃度は海水の1/3程度であったと暗に考えているようである。さらにローマーは、「現生のヌタウナギは海生であるが、腎臓は糸球体を持ちNaを再吸収しており、さらにNa採取のための鰓ポンプを持っている。現生ヌタウナギが海生であるのは順応型の浸透圧調整を2次的に獲得したものであり、祖先のヌタウナギは淡水棲息であった」、とした。現生ヌタウナギの体液イオン濃度は海水とほぼ同じであり、従って、かっては海水の1/3の体液イオン濃度を持っており浸透圧調整型であったが、海に進出するときに浸透圧順応型に進化したことになる。
淡水進化説に基づくと、淡水性の初期硬骨魚類から420Mya頃に条鰭類と肉鰭類が分岐した。410Mya頃に出現した淡水性のCheirolepisは初期の条鰭類であり、一方海に進出したMimia等は現生への子孫を残すことなく滅びた。Cheirolepis の出現以降290~250Myaに真骨魚類 (teleosts)が 出現するまでの間の主要な硬骨魚類は淡水性であった。海棲の真骨魚類であるElopomorphaが出現したのはジュラ紀になってからであり、この時期に淡水性の魚類が新たに塩類細胞を獲得して海棲になったことになる。そして現生淡水魚類が塩類細胞を持つことから、現生淡水魚類は海に進出した魚類が再び淡水域に戻った魚類の子孫ということになる。
こういった魚類の進化史を含め、長いこと淡水進化説が有力であったし、現在でもこの考えへの根強い支持がある。
海洋性魚類の卵の浸透圧調整を行うアクアポリンや卵黄たんぱく質形成遺伝子のvitellogeninといった遺伝子解析からも条鰭類の淡水棲息説が支持されるとする発表が最近なされている。
四肢類のアクアポリンAQP1と淡水魚のアクアポリンaqp1aは似た構造を持っており、ホモロガスと考えられる。海生魚類の卵ではaqp1a とaq1bの発現があるが、一方淡水性魚類ではアクアポリンaq1aの発現はあるが、aq1bの発現はほとんど見られない。卵の海水への適応のためにaq1bが機能を持つようになったと考えられる。これらのことから、四肢類と魚類の共通祖先は、AQP1やaqp1aの祖先型が機能した淡水性であり、全遺伝子重複(3R Hypothesis)により海水適応機能を持つaq1bを持てるようになり、海へ進出出来たと結論した(Tingaud-Sequeira et al. 2008)。
また、淡水に適応していた魚類の卵は、その魚類が海生化する際には卵も海水適応する必要がある。しかし、卵の状態では浸透圧に対処する器官、塩類細胞や腸、腎臓、鰓を持っていない。そのため卵が海水中に放出される前に浸透圧に対応出来る機能を備えた。即ち、卵黄たんぱく質形成遺伝子vitellogenin: Vtgにより誘導される卵黄たんぱく質の成熟に伴いアミノ酸自由基が産生され、これが卵内を水和化する。卵内の水和化により海水中に卵が放出されても脱水状態にならない。Vtgファミリーの詳細解析結果は、条鰭類の系統で起こった全遺伝子重複3R以降に海生適応があったことを示しており、従来の化石記録と矛盾しないと結論した(Finn & Kristoffersen 2007)。
四肢類、海生魚類、淡水性魚類のアクアポリンを比較した報告では、四肢類の腎臓におけるアクアポリンと魚類の卵におけるアクアポリンを対象としている。しかしながらアクアポリンには多様な種類があり、その機能は器官によって大きく異なる。従って、四肢類と魚類の共通祖先がホモロガスなアクアポリンを持っていたにしても同じ淡水適応機能であったとは言い切れないと思われる。
また、条鰭類の系列において3Rが起こる前は淡水棲息であったとすると、肉鰭類と分岐した時点でも、さらには肉鰭類と条鰭類が分岐する前の初期硬骨魚類も淡水棲息であったことになる。従って、条鰭類に3Rが起こる以前に生存していた海生の初期硬骨魚類の存在を説明できない。また、3Rが起こらなかった肉鰭類でも海に進出出来ていたことも説明できない。Vtgに基づいた卵に関する解析は、ジュラ紀に出現した真骨魚類の系統において起こった現象を説明している可能性がある。
従って、遺伝子解析から淡水棲息に言及したこれら二つの論文は、分岐前の初期硬骨魚類が淡水に棲息していたとするローマーの「淡水棲息仮説」を積極的に支持するものではない、と思われる。
初期の魚類が海生か淡水性かに関しては長いこと議論されてきたが、90年代にストロンチュウムのアイソトープ比から淡水堆積物と海洋堆積物とを識別する技術が確立した(Janvier 1996)。その結果最も初期の脊椎動物とされるオルドビス紀の470Mya頃出現したSacabambaspisやArandaspis といったArandaspida類は海生であり、420Mya頃には多くの海底生の、あるいは潟や浅瀬の、さらには表層の海生魚類が出現していることが明らかになった(Janvier 1996)。こういった地質学的観点から最近では初期脊椎動物は海生起源であり、特に顎口類や初期硬骨魚類は海で進化したと結論されているようである。
塩類細胞をいつ獲得したのか?
淡水進化説に基づくと、塩類細胞は新骨魚類になってから、即ちジュラ紀になってから獲得したことになる。
塩類の調節にはNa-K ATPaseと呼ばれる酵素が重要であり、塩類細胞内ではこの酵素の遺伝子を活性化し多量に産生している(Hwang & Lee 2007)。鰓が未発達な胚期には、体表や卵黄嚢上皮に塩類細胞が存在する。また、多くの魚類では卵子や精子といった生殖細胞は、海水の1/3の浸透圧にある体内から急に海水中や淡水中に放出され、細胞レベルですばやく浸透圧調整を行っている。即ち、単細胞レベルでもNa-K ATPaseを産生する遺伝子を活性化することで浸透圧調整を行っている。こういったことから、塩類細胞、乃至は同じような機能を持つ器官は、脊椎動物のかなり初期の段階で既に獲得されていた可能性がある。
さらに現生の海生甲殻類や一部の淡水性昆虫の幼体は古い体制を保持していると考えられるが、塩類様細胞や塩類様器官が見られる(Wichard & Eisenbeis 1979)。また、現生のウミガメや海鳥も塩類腺を持っている。即ち、塩類細胞的な機能を持つ器官は浸透圧調整のためのごく一般的なものであり、節足類にまでたどれる非常に古い器官であることが予想される。
また、脊椎動物の系統では浸透圧調整ホルモンに関連する遺伝子を、機能しないにせよ既にヌタウナギの段階で保持していたことが、現生ヌタウナギの遺伝子解析結果から予想される。ヌタウナギより遅れて古生代の海に出現し、やがて淡水域に侵出したヤツメウナギは現生種と同様体液のイオン濃度は海水のそれのほぼ1/3であったと思われる。従って、体内に流入してくる過剰な水とミネラルイオン類の不足を解消するための機能を当然備えていたはずであり、浸透圧調整ホルモンが働いていたと考えられる。
ヤツメウナギよりもさらに遅れて430~420Myaに棲息していた初期硬骨魚類は海生であり(Janvier 1996)、420Myaまでには条鰭類と肉鰭類に分岐している。現生条鰭類も肉鰭類から進化した四肢類も体液イオン濃度は海水の約1/3に保たれており、共通祖先の初期硬骨魚類の体液濃度も海水の1/3であったと考えられる。従って初期硬骨魚類も浸透圧を調整していたと考えられる。当然浸透圧調整ホルモンが働いており、現生硬骨魚類と同様体内水分が体外へ抜けてしまうことに対処するために海水を鯨飲し、体内で過剰になった一価イオン排出のための塩類細胞を、過剰になった二価イオン排出のための腎臓を使っていたと予想される。
また、肉鰭類の中から365Mya頃には両生類が生まれるが、これら初期四肢類の多くは海岸や汽水域といった海生の環境に棲息していたことが化石から確認されている。さらには初期四肢類のBaphetidae は淡水にも海水にも棲んでおり、頭骨化石形状から塩類腺を持っていた可能性があるとされる(クラック)。これは初期四肢類の祖先の肉鰭類が浸透圧調整方式を採用していたことを示唆する。
腎臓の機能はホメオスタシス保持であり、本来は体内の水とミネラルの制御・調整である(Ogasawara & Ichikawa 2009)。海生頭索類のナメクジウオ(Ruppert 1994)や海生円口類のヌタウナギが糸球体に類似する器官を持っていることから、腎臓の機能は体内イオン調整であり、そのために水の制御、即ちポンプ機能を持つのであり、ポンプ機能を持つことが淡水棲息を意味するのではないと思われる。むしろ原尿に含まれるイオン類等を再吸収する尿細管、特に遠位尿細管の発達が淡水棲息と関係する(内山 他 2000)。即ち、イオン類が少ない淡水環境で棲息するために再吸収機能を高める必要があり、発達した尿細管が必要である。尿細管の機能は、環境によって恐らくかなり容易に変更できるであろう。実際海生魚類では遠位尿細管が縮小するか、消失しているものが多い。
脊椎動物は、かなり初期の段階で海への適応のために塩類細胞、乃至は似たような機能を持つ器官を発達させており、450~420Mya頃棲息していたと考えられる初期硬骨魚類は海生で、塩類細胞、あるいはそれに近い機能を持つ器官や腎臓を使って浸透圧調整を行っていたと考えられる。また、腎臓のポンプ機能は祖先の淡水棲息を必ずしも意味するものではない、といえる。
窒素廃棄物の処理
食餌として摂りいれたタンパク質をアミノ基に代謝する際に有毒のアンモニアが生じるが、アンモニアは毒性が強いので速やかに体内から排出する必要がある。アンモニアが水に容易に溶け込むため、鰓はアンモニアを排出する器官としても機能するようになった。水に囲まれている魚類や水棲両生類、及び陸棲両生類の幼体は、アンモニアを鰓や一部は皮膚から容易に体外に放出できる。
アンモニア排出に関する鰓上皮細胞の機能面でのモデルがいくつか提案されている(Weihrauch et al. 2009)(Wright & Wood 2009)(Nakada et al. 2007)(Wilkie 2002)。淡水性と海生の条鰭類のアンモニア排出モデルと軟骨魚類の尿素排出モデルを以下に示す。
古生代の魚類における恒常性維持
軟骨魚類やシーラカンス等一部を除くと、現生魚類の多くは体内イオン濃度をほぼ海水のイオン濃度の1/3程度に保つために鰓や塩類細胞、あるいは腎臓により浸透圧調整を行っている。これらの器官はNPs:natriuretic peptidesなどの浸透圧調整ホルモンによって制御されている。
現生ヤツメウナギは淡水性の硬骨魚と類似した浸透圧調節機構をもっている。古生代に無顎類ヌタウナギより遅れて545Myaには出現したと考えられるヤツメウナギは当時は海生であり(Shu et al. 1999)、その後淡水域に進出している。従って、初期のヌタウナギは浸透圧調整ホルモン遺伝子を持っていたと予想され、海生から淡水へと侵出したヤツメウナギが、現生淡水性魚類に類似した浸透圧調整ホルモンを産生していた可能性は大きいと考えられる(Bartels & Potter 2004)。
ヤツメウナギ以外にも古生代に海生であった棘魚類、それにあまり多くはないが板皮類はいずれも淡水域にも進出している。従って古生代の魚類は既に浸透圧調整機能を保持していた可能性がある。また、体液イオン濃度を海水のほぼ1/3に保っている現生四肢類や条鰭類の共通祖先である初期硬骨魚類も同じ体液イオン濃度であったと考えられる。即ち、古生代の硬骨魚類も海生にせよ淡水生にせよ浸透圧調整を行っていたと考えられ、浸透圧調整ホルモン類も機能していたと考えられる。
体液イオン濃度を海水のほぼ1/3に保つ魚類は浸透圧調整型であり、浸透圧が変化した場合浸透圧を調整する専用の器官により体液濃度が保たれるので、体を構成する各細胞は浸透圧変化の影響をほとんど受けないで済む。一方、軟骨魚類は浸透圧順応型であり、浸透圧が変化した場合、体液や細胞内の浸透圧を総て変える必要があり、従って浸透圧順応型の方が浸透圧調整型よりも浸透圧変化への対応がより困難と考えられる。淡水に適応している軟骨魚類が少ない一因は、体内浸透圧を淡水に合わせるのが困難なためと考えられる。
古生代の初期魚類の分岐時期や海・淡水の分布や放散を考慮すると、板皮類、棘魚類の浸透圧変化への対応を類推することが出来ると思われる。化石記録から、板皮類は主に海の湾岸を生息場所にして多様化していることが分かっている。一方、棘魚類は最初は海に出現したが、ほどなく淡水域に進出し、主に淡水域で放散・繁栄している。
板皮類と軟骨魚類はオルドビス紀末には出現しており、最近板皮類のarthrodireが胎生であったことが明らかにされ(Long et al. 2009)、板皮類と軟骨魚類の類縁性が再確認された。恐らく板皮類も当時の軟骨魚類と同様尿素により体液の浸透圧を高める浸透圧順応型の方式を採用していたと思われる。淡水域に進出するには、体を構成している総ての細胞の内部機能を変える必要があり、このため板皮類も軟骨魚類と同様に淡水域への進出はそれほど容易ではなかったと思われる。
一方、海生として出現した棘魚類は後に淡水域へ進出し繁栄しており、板皮類や軟骨魚類より淡水域への進出が容易だったと思われる。従って、棘魚類は初期硬骨魚類と同様体液イオン濃度を海水の約1/3に保つ浸透圧調整型の方式を採用していた可能性がある。
なお、汽水域のように急激に塩分濃度が変化する場所では板皮類は強固な外皮により、軟骨魚類は直腸腺などで微調整することにより、一時的な塩分濃度変化に対応したと考えられる。ほぼ海水と同濃度の体液を持っているヌタウナギでは体表の粘液で一時的な外界の塩分濃度変化に対応していたであろう。
初期魚類進化の場は海だったのか、淡水だったのか?
初期脊椎動物が海域で進化したのか、淡水域で進化したのかに関する議論が長いこと為されてきた(Bray 1985)(Griffith 1987)。多くの初期魚類化石が淡水域で積層したと考えられたOld Red Sandstoneから出土していた。また海で堆積した地層からも化石が出土するが、成体がほとんどであり、海生であったにしても現生の原始的魚類の生活史と同様に淡水で繁殖し幼体時期を過ごした後に海へ移動して成体になったと考えられた(Griffith 1987)。
Smithは「腎臓に見られる糸球体は過剰な水の存在、即ち淡水棲息を裏付ける。軟骨魚類は四肢類以上に複雑な腎臓であるが、糸球体を持つ腎臓なのでかっては淡水性であったし、軟骨魚類の祖先とされる板皮類も最初は淡水性であった」と主張している。この考えに基づきローマーは、「現生海生魚類では、体液の塩類濃度が高くなるためポンプによる水の排出は必要ないはずなのに働いている。この不都合を解消するために二つの方法を開発した。一つは硬骨魚類に見られる塩類細胞であり、二つ目はサメ類に見られるように尿素濃度を高めて体外の塩類濃度と釣り合いを保つ方法である。こういった特殊な機能を発達させたことを説明できるのは、このような腎臓を発達させた祖先的脊椎動物は淡水中に棲んでいたからである」と考えた。そして「ポンプで絶えず水をくみ出す脊椎動物の腎臓は、淡水に棲む魚において発達したものである」と結論した。
ローマーの仮説に基づくと、「古生代の初期魚類は淡水に棲息しており、塩類細胞を持っていなかった。そのため海に進出するときに、塩類細胞を獲得するか、軟骨魚類のように尿素によって浸透圧に対応する必要があった」、と結論される。従って、軟骨魚類を含め初期魚類は淡水域に棲息しており、ポンプ機能の腎臓を持っており、従ってその体液イオン濃度は海水の1/3程度であったと暗に考えているようである。さらにローマーは、「現生のヌタウナギは海生であるが、腎臓は糸球体を持ちNaを再吸収しており、さらにNa採取のための鰓ポンプを持っている。現生ヌタウナギが海生であるのは順応型の浸透圧調整を2次的に獲得したものであり、祖先のヌタウナギは淡水棲息であった」、とした。現生ヌタウナギの体液イオン濃度は海水とほぼ同じであり、従って、かっては海水の1/3の体液イオン濃度を持っており浸透圧調整型であったが、海に進出するときに浸透圧順応型に進化したことになる。
淡水進化説に基づくと、淡水性の初期硬骨魚類から420Mya頃に条鰭類と肉鰭類が分岐した。410Mya頃に出現した淡水性のCheirolepisは初期の条鰭類であり、一方海に進出したMimia等は現生への子孫を残すことなく滅びた。Cheirolepis の出現以降290~250Myaに真骨魚類 (teleosts)が 出現するまでの間の主要な硬骨魚類は淡水性であった。海棲の真骨魚類であるElopomorphaが出現したのはジュラ紀になってからであり、この時期に淡水性の魚類が新たに塩類細胞を獲得して海棲になったことになる。そして現生淡水魚類が塩類細胞を持つことから、現生淡水魚類は海に進出した魚類が再び淡水域に戻った魚類の子孫ということになる。
こういった魚類の進化史を含め、長いこと淡水進化説が有力であったし、現在でもこの考えへの根強い支持がある。
海洋性魚類の卵の浸透圧調整を行うアクアポリンや卵黄たんぱく質形成遺伝子のvitellogeninといった遺伝子解析からも条鰭類の淡水棲息説が支持されるとする発表が最近なされている。
四肢類のアクアポリンAQP1と淡水魚のアクアポリンaqp1aは似た構造を持っており、ホモロガスと考えられる。海生魚類の卵ではaqp1a とaq1bの発現があるが、一方淡水性魚類ではアクアポリンaq1aの発現はあるが、aq1bの発現はほとんど見られない。卵の海水への適応のためにaq1bが機能を持つようになったと考えられる。これらのことから、四肢類と魚類の共通祖先は、AQP1やaqp1aの祖先型が機能した淡水性であり、全遺伝子重複(3R Hypothesis)により海水適応機能を持つaq1bを持てるようになり、海へ進出出来たと結論した(Tingaud-Sequeira et al. 2008)。
また、淡水に適応していた魚類の卵は、その魚類が海生化する際には卵も海水適応する必要がある。しかし、卵の状態では浸透圧に対処する器官、塩類細胞や腸、腎臓、鰓を持っていない。そのため卵が海水中に放出される前に浸透圧に対応出来る機能を備えた。即ち、卵黄たんぱく質形成遺伝子vitellogenin: Vtgにより誘導される卵黄たんぱく質の成熟に伴いアミノ酸自由基が産生され、これが卵内を水和化する。卵内の水和化により海水中に卵が放出されても脱水状態にならない。Vtgファミリーの詳細解析結果は、条鰭類の系統で起こった全遺伝子重複3R以降に海生適応があったことを示しており、従来の化石記録と矛盾しないと結論した(Finn & Kristoffersen 2007)。
四肢類、海生魚類、淡水性魚類のアクアポリンを比較した報告では、四肢類の腎臓におけるアクアポリンと魚類の卵におけるアクアポリンを対象としている。しかしながらアクアポリンには多様な種類があり、その機能は器官によって大きく異なる。従って、四肢類と魚類の共通祖先がホモロガスなアクアポリンを持っていたにしても同じ淡水適応機能であったとは言い切れないと思われる。
また、条鰭類の系列において3Rが起こる前は淡水棲息であったとすると、肉鰭類と分岐した時点でも、さらには肉鰭類と条鰭類が分岐する前の初期硬骨魚類も淡水棲息であったことになる。従って、条鰭類に3Rが起こる以前に生存していた海生の初期硬骨魚類の存在を説明できない。また、3Rが起こらなかった肉鰭類でも海に進出出来ていたことも説明できない。Vtgに基づいた卵に関する解析は、ジュラ紀に出現した真骨魚類の系統において起こった現象を説明している可能性がある。
従って、遺伝子解析から淡水棲息に言及したこれら二つの論文は、分岐前の初期硬骨魚類が淡水に棲息していたとするローマーの「淡水棲息仮説」を積極的に支持するものではない、と思われる。
初期の魚類が海生か淡水性かに関しては長いこと議論されてきたが、90年代にストロンチュウムのアイソトープ比から淡水堆積物と海洋堆積物とを識別する技術が確立した(Janvier 1996)。その結果最も初期の脊椎動物とされるオルドビス紀の470Mya頃出現したSacabambaspisやArandaspis といったArandaspida類は海生であり、420Mya頃には多くの海底生の、あるいは潟や浅瀬の、さらには表層の海生魚類が出現していることが明らかになった(Janvier 1996)。こういった地質学的観点から最近では初期脊椎動物は海生起源であり、特に顎口類や初期硬骨魚類は海で進化したと結論されているようである。
塩類細胞をいつ獲得したのか?
淡水進化説に基づくと、塩類細胞は淡水に棲息していた新骨魚類が海に進出するとき、即ちジュラ紀になってから獲得したことになる。
塩類の調節にはNa-K ATPaseと呼ばれる酵素が重要であり、塩類細胞内ではこの酵素の遺伝子を活性化し多量に産生している(Hwang & Lee 2007)。鰓が未発達な胚期には、体表や卵黄嚢上皮に塩類細胞が存在する。また、多くの魚類では卵子や精子といった生殖細胞は、海水の1/3の浸透圧にある体内から急に海水中や淡水中に放出され、細胞レベルですばやく浸透圧調整を行っている。即ち、単細胞レベルでもNa-K ATPaseを産生する遺伝子を活性化することで浸透圧調整を行っている。こういったことから、塩類細胞、乃至は同じような機能を持つ器官は、脊椎動物のかなり初期の段階で既に獲得されていた可能性がある。
さらに現生の海生甲殻類や一部の淡水性昆虫の幼体は古い体制を保持していると考えられるが、塩類様細胞や塩類様器官が見られる(Wichard & Eisenbeis 1979)。また、現生のウミガメや海鳥も塩類腺を持っている。即ち、塩類細胞的な機能を持つ器官は浸透圧調整のためのごく一般的なものであり、節足類にまでたどれる非常に古い器官であることが予想される。
また、脊椎動物の系統では浸透圧調整ホルモンに関連する遺伝子を、機能しないにせよ既にヌタウナギの段階で保持していたことが、現生ヌタウナギの遺伝子解析結果から予想される。ヌタウナギより遅れて古生代の海に出現し、やがて淡水域に侵出したヤツメウナギは現生種と同様体液のイオン濃度は海水のそれのほぼ1/3であったと思われる。従って、体内に流入してくる過剰な水とミネラルイオン類の不足を解消するための機能を当然備えていたはずであり、浸透圧調整ホルモンが働いていたと考えられる。
ヤツメウナギよりもさらに遅れて430~420Myaに棲息していた初期硬骨魚類は海生であり(Janvier 1996)、420Myaまでには条鰭類と肉鰭類に分岐している。現生条鰭類も肉鰭類から進化した四肢類も体液イオン濃度は海水の約1/3に保たれており、共通祖先の初期硬骨魚類の体液濃度も海水の1/3であったと考えられる。従って初期硬骨魚類も浸透圧を調整していたと考えられる。当然浸透圧調整ホルモンが働いており、現生硬骨魚類と同様体内水分が体外へ抜けてしまうことに対処するために海水を鯨飲し、体内で過剰になった一価イオン排出のための塩類細胞を、過剰になった二価イオン排出のための腎臓を使っていたと予想される。
また、肉鰭類の中から365Mya頃には両生類が生まれるが、これら初期四肢類の多くは海岸や汽水域といった海生の環境に棲息していたことが化石から確認されている。さらには初期四肢類のBaphetidae は淡水にも海水にも棲んでおり、頭骨化石形状から塩類腺を持っていた可能性があるとされる(クラック)。これは初期四肢類の祖先の肉鰭類が浸透圧調整方式を採用していたことを示唆する。
腎臓の機能はホメオスタシス保持であり、本来は体内の水とミネラルの制御・調整である(Ogasawara & Ichikawa 2009)。海生頭索類のナメクジウオ(Ruppert 1994)や海生円口類のヌタウナギが糸球体に類似する器官を持っていることから、腎臓の機能は体内イオン調整であり、そのために水の制御、即ちポンプ機能を持つのであり、ポンプ機能を持つことが淡水棲息を意味するのではないと思われる。むしろ原尿に含まれるイオン類等を再吸収する尿細管、特に遠位尿細管の発達が淡水棲息と関係する(内山 他 2000)。即ち、イオン類が少ない淡水環境で棲息するために再吸収機能を高める必要があり、発達した尿細管が必要である。尿細管の機能は、環境によって恐らくかなり容易に変更できるであろう。実際海生魚類では遠位尿細管が縮小するか、消失しているものが多い。
脊椎動物は、かなり初期の段階で海への適応のために塩類細胞、乃至は似たような機能を持つ器官を発達させており、450~420Mya頃棲息していたと考えられる初期硬骨魚類は海生で、塩類細胞、あるいはそれに近い機能を持つ器官や腎臓を使って浸透圧調整を行っていたと考えられる。また、腎臓のポンプ機能は祖先の淡水棲息を必ずしも意味するものではない、といえる。
窒素廃棄物の処理
食餌として摂りいれたタンパク質をアミノ基に代謝する際に有毒のアンモニアが生じるが、アンモニアは毒性が強いので速やかに体内から排出する必要がある。アンモニアが水に容易に溶け込むため、鰓はアンモニアを排出する器官としても機能するようになった。水に囲まれている魚類や水棲両生類、及び陸棲両生類の幼体は、アンモニアを鰓や一部は皮膚から容易に体外に放出できる。
アンモニア排出に関する鰓上皮細胞の機能面でのモデルがいくつか提案されている(Weihrauch et al. 2009)(Wright & Wood 2009)(Nakada et al. 2007)(Wilkie 2002)。淡水性と海生の条鰭類のアンモニア排出モデルと軟骨魚類の尿素排出モデルを以下に示す。

体内から体外へアンモニアを抽出するRhタンパク質には3種類あり、赤血球からアンモニアを抽出するのがRhagであり、そのアンモニアを鰓細胞に取り込むのがRhbgであり、さらに鰓細胞膜と通して体外に抽出するのがRhcgである。RBC: red blood cell。
From Wright & Wood 2009

体内から体外へのアンモニア抽出には3つのルートがある。Rhタンパク質に依存したルートと細胞間を通過するルートがある。その他にミトコンドリアを多数含むルートもある。
NH3排出のほとんどはpv cellsが担う。図4とは逆に鰓細胞の右側が体外である。
pv cell: pavement cell、MR cell: mitochondria rich cell。
From Weihrauch et al. 2009
なお、鰓からのアンモニア放出は容易であるが、その放出メカニズムに関しては議論が進行中である(Nakada et al. 2007)。
尿素はアンモニアよりも毒性が弱いし水に溶けやすく、細胞内外液に分散しやすい。そのため軟骨魚類はアンモニアを尿素に変えて体内外の浸透圧差を調整している(兵藤 他 2008)(内山 他 2009)。さらに、軟骨魚類以外の現生条鰭類でも高温の水域や強いアルカリ性の水域に棲むテラピア類等は窒素老廃物を尿素の形で鰓から排出している。あるいは脱水やpH変化といったストレスによって、通常のアンモニアから速やかに尿素へと排出様式を変えたり、鰓の未発達な幼魚では窒素廃棄物のほとんどを尿素の形で処理し、成体になり鰓が発達すると主にアンモニアで処理する条鰭類も多い(Kaneko 2006)( Hyodo et al. 2004)。
軟骨魚類はもとよりほとんどの条鰭類は、窒素廃棄物の大部分をアンモニアの形で鰓から排出するが、同時に尿素を産生し、排出している。一般に海生条鰭類の方が尿素排出の比率が高いとされる。軟骨魚類のアンモニア排出に関する鰓細胞の機能は海生の硬骨魚類とは異なっており、細胞内での尿素の産生が可能である。
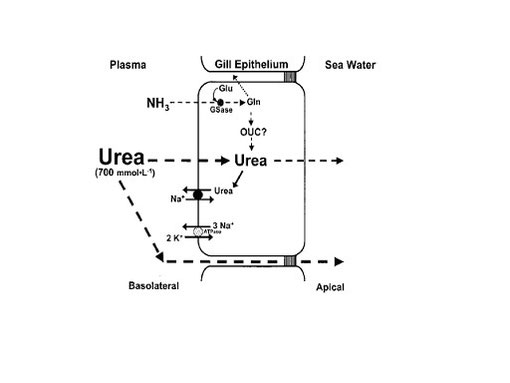
アンモニアは海生魚類の鰓細胞におけるのと似た機構で鰓細胞に取り込まれる。鰓細胞内に取り込まれたアンモニアからGSaseによってグルタミンが産生される。グルタミンは肝臓に移動しオルチニン尿素回路に取り込まれるか、鰓細胞内に留まり、尿素に合成変換される。鰓細胞内で合成された尿素は尿素トランスポーターによって基底膜から抽出されるが、鰓細胞の基底膜はコレステロール:燐脂質に富んでおり、基底膜からの尿素消失が抑制される。そのため基底膜近傍に尿素の高濃度勾配が形成される。尿素トランスポーターの活性度はNa+に依存する。 From Wilkie 2002
脊椎動物は、水圏から陸上に棲息場所を移すときに代謝の結果生じる窒素老廃物をアンモニアの形で周囲の水中に排出することが困難になった。陸棲の両生類や哺乳類はアンモニアを肝臓で毒性の低い尿素に変えて腎臓に送り、体内からの水の消耗を防ぐために濃縮して尿として排出する。また、爬虫類や鳥類はアンモニアを水にほとんど溶けない尿酸に変えて固体として体外に排出することで体内からの水の損失をさらに抑制している。
図7に尿素産生経路のモデルを示す。脊椎動物では、尿素は肝臓でオルニチンー尿素サイクルの窒素同化経路によって合成される。現生の軟骨魚類とシーラカンスの尿素サイクルではカルバミルリン酸合成酵素Ⅲ:CPSⅢが使われているが、四肢類やハイギョではCPSⅠが使われている(Haskins et al. 2008)。CPSⅠもCPSⅢも共に最終産物は尿素である。カルバミルリン酸合成酵素のアミノ酸配列比較からCPSⅡが祖形であり、魚類に見られるCPSⅢを経て、両生類になった段階で陸棲脊椎動物に見られるCPSⅠへと進化してきたとされたが(Hong et al. 1994)、最近の報告では無脊椎動物でもCPSⅢが機能していることが明らかになった(Haskins et al. 2008)。この一連の進化は、主に尿素サイクルにおいてcarbomyl-phospate: CP合成に関与する酵素N-acetylglutamate: NAG におけるアロステリックな反応で起こったと考えられる。
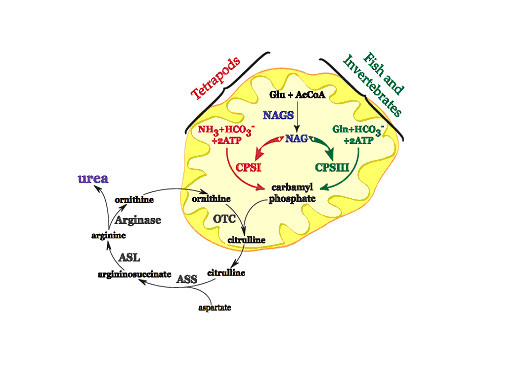
尿素サイクルの最初の3つの酵素NAGS、CPSⅠ、CPSⅢはミトコンドリア内に、他の3つASS、 ASL、 Arginaseは細胞質内に存在する。哺乳類と両生類はアンモニア、重炭酸塩、ATPからCPを産生する酵素CPSⅠを持つ。NAGはCPSⅠのアロステリックな活性体である。CPSⅢはグルタミナーゼ、重炭酸塩、ATPからCPを産生する酵素であり、魚類と無脊椎動物で機能している。酵素CPSⅢはNAGによって活性度が増加する。
CP:carbamyphospate, NAGS:N-acetylgultamate syhthase, NAG:N-acetylgutamate, CPSⅠ:carbamylphospate synthetase, CPSⅢ: carbamylphospate synthetaseⅢ, OTC:ornithine transcarbamylase, ASS:argininosuccinate synthase, ASL:argininosuccuante lyase. From Haskins et al. 2008
オルニチン回路による尿素の産生は初期顎口類の段階で獲得したと考えられたが(Bray 1985)、それよりも前の無脊椎動物段階で既に獲得されていたことになる。従って、条鰭類、肉鰭類、軟骨魚類の共通祖先であった初期魚類がすでに尿素産生機能を持ち、尿素の形で排出する方式を獲得していたと考えられる。
古生代に出現した初期軟骨魚類は、祖先の尿素産生のシステムを継承し、現生軟骨魚類と同様に尿素による浸透圧制御を行う浸透圧順応型の魚類だったと思われる。
一方、硬骨魚類の系統は、初期硬骨魚の段階で既に体液のイオン濃度を海水のおよそ1/3に保つ浸透圧調整型の魚類であった。浸透圧調整型のシステムはヤツメウナギの段階で機能し始めたものであり、浸透圧調整のための尿素を必要とせず、従って窒素廃棄物をアンモニアの形で排出していたと考えられる。即ち、硬骨魚類の系統は、ヤツメウナギから初期硬骨魚類の時代まで、非常に長期間にわたって尿素の産生を必要としないアンモニアによる窒素廃棄物の処理を行っていたことになる。そして現生の硬骨魚類においても尿素の産生を必要としないアンモニアによる窒素廃棄物の処理を行っている。
しかしながら初期硬骨魚類から分岐した肉鰭類の系統では、四肢類になった段階では尿素産生システムを再機能させた。また、現生条鰭類は、ストレス下や幼体時に尿素を産生するとされるが、平常時でも窒素廃棄物の一部を尿素の形で鰓から排出する機能を保持している。アンモニアの形で窒素廃棄物を処理するようになっても、魚類は無脊椎動物時代に獲得した尿素産生機能を非常に長い期間に渡って保持してきたことになる(Walsh 1997)(McDonald et al. 2006)。
代謝のためのエネルギーという観点では、蛋白質をアンモニアに変えるよりも尿素に変えるほうが不利であるにも関わらず、尿素産生の機能を魚類が長期間保持してきた理由は、あまりはっきりしない。アンモニアは毒性が強いので、鰓が充分に発達していない幼体の段階ではアンモニアの毒性に耐えられないため尿素の形にする必要があり、そのため尿素産生の機能を保持する必要があったと思われる。
また、水棲であった無脊椎動物段階で代謝エネルギーの点でアンモニア産生よりも不利な尿素産生機能を持った理由もあまりはっきりしない。先述のように、高温環境に棲息する現生テラピアの1種は、窒素廃棄物として尿素を産生し鰓から排出している。このことは、尿素産生機能が、第1章の図11に見たように、オルドビス紀初期の40℃という高温の海表面における生存への適応として獲得された可能性を示唆していると思われる。
陸棲化に伴う腎機能の拡大
硬骨魚類は大半の窒化廃棄物をアンモニアの形で処理していたが、尿素産生機能を失わなかったし、尿素の形で鰓から排出する機能も保持してきた。一方、腎臓は、本来水と塩分の調整機能を持つ浸透圧調整のための器官であった。従って、硬骨魚類の腎臓に窒素老廃物の処理機能はない(McDonald et al 2006)。尿素のような窒化廃棄物の排出は陸棲化に伴い腎臓に付加された機能である(Ogasawara & Ichikawa 2009)。
実際、現生ハイギョの腎臓は尿素の形での窒化廃棄物の排出機能を持っていない(クラック)。ハイギョは、乾季の夏眠中は老廃物を体内に溜め、雨季に水中で鰓から排出する。即ち、肉鰭類を含めた硬骨魚の系統では尿素を作ることは出来たが、腎臓で濃縮する機能は陸棲化まで未発達の状態だったと思われる。恐らく鰓を持つ初期四肢類もハイギョと同様の方式で窒化廃棄物をアンモニアの形で鰓を使って処理を行っていたと思われる(クラック)。陸棲化に伴う鰓の縮小、消失に伴って、肝臓による窒化廃棄物の尿素化と腎臓による尿素処理の機能が増大していったと考えられる。
陸棲化に伴う鰓の消失
水棲動物であれば、鰓は軟体動物、節足動物、環形動物、脊索・脊椎動物の魚類や一部の両生類にも見られる一般的な器官である。水棲動物の鰓の主要な機能は、水中の酸素を体内に取り込み、体内の二酸化炭素を排出するガス交換器官であるが(Gilmour & Perry 2009)、その初期にはナメクジウオや尾索類に見られるように摂食と呼吸のためであった。鰓はその機能を満たすため広い表面積を持ち、鰓の表面では鰓上皮細胞がその頂端膜を直接環境水と接し、基底膜を多数の血管網に接している。その構造上浸透圧の影響を受けやすく、そのために浸透圧調整のための最前線の器官にもなっている。浸透圧調整器官として特に鰓の鰓弁部には多くの塩類細胞が存在している。
鰓は水棲には必須の器官であるが、その構造上乾燥に対して非常に脆弱である。従って、ハイギョは乾季に代謝を下げ鰓を保護するために粘液性の繭に篭る生活を採用している。トビハゼなどの現生両性魚類は大気中でも口中に水を保持し、鰓呼吸の維持と乾燥から守る機能を進化させている。
デボン紀末に出現した初期四肢類は鰓を持っていたが、鰓を乾燥から守る機能を持っていたのかは、はっきりしない。また、デボン紀末から石炭紀にかけて出現した新四肢類も鰓を保護する機能を持っていたのかは、はっきりしない。恐らく鰓を保護する機能を持たないのも、持つのも出現していたと思われる。
鰓の保護機能を進化させなかった四肢類では、陸棲化に際して鰓の縮小・消失と肺呼吸機能の向上に加え、腎臓による窒化廃棄物処理の獲得が急激に起こったと予想される。一方、鰓を乾燥から守る器官を発達させた四肢類では、肺呼吸機能は未発達のままであり、腎臓による窒化廃棄物処理の機能の進化もほとんど起こらず、鰓によるアンモニア排出を継続し、非常に限定された陸棲しか出来なかったであろう。
ある程度の陸棲が可能であったとされるアカントステガやイクチオステガは鰓を持っており、鰓を乾燥から守る何らかの機構を持っていた可能性がある。通気孔が上向きの孔を持ち、その位置が頭頂であったことは、泥濘中での鰓の保護のためであったとされる。一方、この構造は鰓を乾燥から守る機能を持たせるのに都合が良かったと考えられる。即ち、鰓蓋を閉じれば鰓部に水を溜めて置くことが可能であったであろう。
陸を目指した初期四肢類の多くはデボン紀末の大絶滅を生き残れなかった。一方、「ローマーの空隙」の直後に出現した新四肢類の多くは水棲であった(Coates)。これは、これら初期の四肢類の多くが陸上でも鰓に頼る方式を採用しており、肺機能が未発達のままであり、腎臓に新たに窒化廃棄物処理の機能を付加しなかった可能性を示唆している。
「ローマーの空隙」の時期に鰓機能の低下・消失に伴い、肺機能の向上と腎臓への新機能の付加を急激に達成した一部の四肢類のみが、「ローマーの空隙」後に一層の陸棲化を進めることが出来たと考えられる。
陸棲化に伴う皮膚からの水の蒸散
水圏に棲息する場合浸透圧調整とそれに関与する塩類細胞は重要であったが、完全に陸棲化した場合には浸透圧の問題は無くなり、塩類細胞も不要になった。代わりに体からの水分の蒸散を抑制する機能へと置き換わる。即ち、陸棲化に際して表皮から水分が蒸散するのを抑制する方向に選択が働いた。
浸透圧に対処するために、海生の魚類は表皮から水が流出するのを防ぐ機能を、淡水性の魚類は表皮から水が流入するのを防ぐ機能を発達させている。従って、陸棲化に際して海生魚類の方が淡水性魚類よりも皮膚機能が陸棲化に有利であった可能性がある。一方、陸棲化の前段階として浅瀬で背側が曝気した状態に置かれたとき、淡水性魚類は腹側では水の流入を抑制する機能を保持したまま、背側では水の放散を抑制する方向に変化する必要があった。そのため粘液で皮膚を被い乾燥を防ぐ方式を進化させたのであろうが、この方式では完全な陸棲化は困難であったろう。現生の無尾両生類のほとんどは淡水性であり、発達した粘液腺を持ち、一方腹側の皮膚から体内に水を取り込んでいる。また、体内からかなりの量の水分が失われても生き延びることが可能な、乾燥に耐えられる代謝システムを持っている(奥野)。
浸透圧に対する皮膚を含めた代謝システムの違いは、四肢類が淡水からと海水からで別々に上陸し、前者が両生類へ、後者が羊膜類へと進化したとする説(ジンマー)の一つの根拠になるであろう。
まとめ
脊椎動物は、かなり初期の段階で海への適応のために塩類細胞、乃至は似たような機能を持つ器官を発達させていた。430~420Mya頃棲息していた初期硬骨魚類は海生で、塩類細胞や腎臓を使って浸透圧調整を行っており、初期硬骨魚類から分岐した肉鰭類もこういった特性を備えていたと考えられる。浸透圧調整システムを獲得していたことにより、肉鰭類も海ばかりでなく淡水域へも進出が可能になった。
食餌として摂りいれたタンパク質を代謝する際に生じる窒化廃棄物を、魚類はアンモニアの形で鰓や一部は皮膚から体外に放出している。哺乳類は有毒なアンモニアをオルニチン回路により尿素に変えて、爬虫類や鳥類は尿酸に変えて体外に排出している。軟骨魚類や鰓の未発達な幼魚では窒化廃棄物を尿素の形で処理しており、オルニチン回路による尿素の産生は無顎類の段階で既に獲得していたと考えられる。
腎臓の機能は、本来は水と塩分の調整であるが、陸棲化に伴い腎臓の尿素排出機能が付加された。
初期四肢類の多くはデボン紀末に絶滅し、「ローマーの空隙」の直後に出現した四肢類は初期四肢類とは異なった形態を持ち、多くは水棲であった。「ローマーの空隙」の時期に鰓機能の消失に伴い、肺機能の向上、及び腎臓への尿素処理機能の付加を急激に達成した一部の四肢類のみが、「ローマーの空隙」後に一層の陸棲化を進めることが出来た。
 魚が陸上を歩くまで
魚が陸上を歩くまで